
Ritardo Pfizer. Ue e Italia non transigono e chiedono il rispetto dei patti
Nei giorni scorsi, da parte di Pfizer era arrivato un appello affinché si lavorasse più velocemente per l’approvazione degli altri vaccini ancora nelle ultime fasi…



Nei giorni scorsi, da parte di Pfizer era arrivato un appello affinché si lavorasse più velocemente per l’approvazione degli altri vaccini ancora nelle ultime fasi…
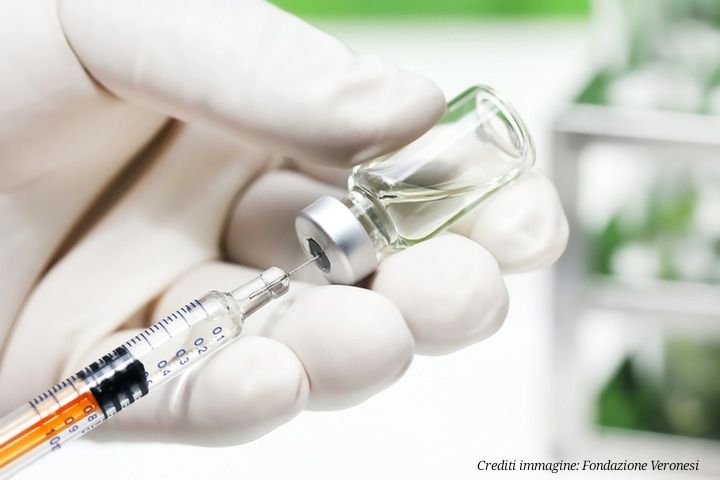
Crediti immagine: Ansa È dell’8 Gennaio 2021 la pubblicazione, da parte di BioNTech sulla rivista Science, di un vaccino sperimentale per la cura della Sclerosi Multipla….
Questa mattina ha avuto inizio la campagna vaccinale anti Covid-19 presso il Policlinico Universitario “G. Martino”. In Sicilia sono giunte nei giorni scorsi le prime…

E’ arrivato l’attesissimo “Vaccine Day” detto anche “V-Day” per tutta l’Europa e l’Italia. Un giorno di svolta, che segna l’inizio della rimonta contro la pandemia….
Sta per partire la campagna per la vaccinazione anti Covid-19. L’Azienda Ospedaliera Universitaria Policlinico “G. Martino”, fa sapere con una nota che è possibile trovare…

Le numerose scene di assembramenti a cui abbiamo assistito nell’ultimo fine settimana e l’aumento del rapporto tamponi-positivi sarebbero le cause di una rinnovata necessità da…
Il diabete mellito di tipo 2 e l’obesità rappresentano due entità cliniche spesso correlate, oggi dilaganti fra la popolazione mondiale, tanto da costituire una vera…

Recentemente la corsa al vaccino anti-SARS-CoV2 sembra aver ricevuto un’accelerata decisiva: in studi di fase tre, i due sieri delle case farmaceutiche americane Pfizer e…

Una luce in fondo al tunnel si è accesa con l’annuncio dell’efficacia al 90% del vaccino prodotto dall’industria farmaceutica americana Pfizer in collaborazione con la…