Utero artificiale: la tecnologia è pronta, noi?
Un problema di certo non trascurabile nel mondo globalizzato è la sopravvivenza dei bambini nati pre-termine, che possono soffrire di complicazioni gravi dovute alla mancanza…


Un problema di certo non trascurabile nel mondo globalizzato è la sopravvivenza dei bambini nati pre-termine, che possono soffrire di complicazioni gravi dovute alla mancanza…

Il termine superfetazione deriva dal latino superfetare (“concepire di nuovo”), il suo reale significato è quello di una “fecondazione in più” o “fecondazione ulteriore”. Il…
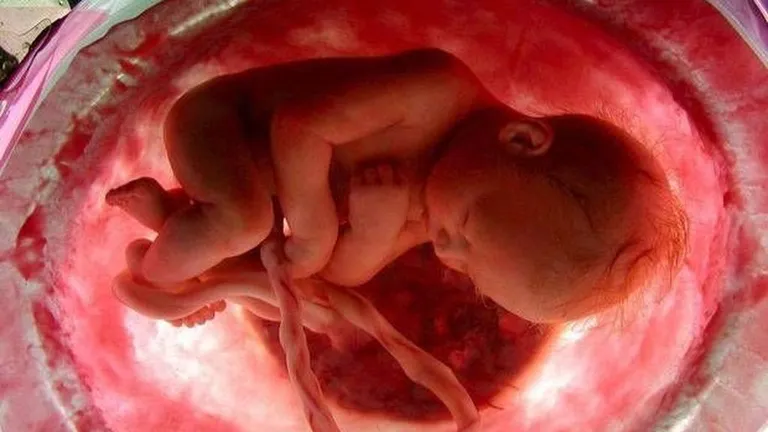
L’intera gestazione spesso viene scambiata da molti per un miracolo. Questa in realtà viene resa possibile, dalla fecondazione al parto, grazie a dei processi chimico-fisici…
Spesso, dietro la bontà degli alimenti come carne, verdura e frutta, che consumiamo giornalmente, potrebbe celarsi uno tra i tanti microscopici patogeni che popolano i…
Scoprire un nuovo gruppo sanguigno è importante perché, in questo modo, è possibile effettuare correttamente molte diagnosi. Il gruppo sanguigno più recentemente scoperto è stato…

Pillole per lei, ma anche per lui. Tra qualche tempo sarà possibile ampliare l’orizzonte della contraccezione con l’introduzione sul mercato della pillola anticoncezionale maschile, avendo…

In uno scenario mondiale in cui la pandemia di COVID-19 desta preoccupazioni e miete nuove vittime sono molte le questioni lasciate irrisolte. Tra queste, la…

Dalla notte dei tempi, esistono decine e decine di credenze popolari sui segnali che possano predire se il neonato sarà maschio o femmina. La presenza o meno di…

La gravidanza gemellare è un evento affascinante che è tuttora oggetto di intenso studio. A differenza di numerosi mammiferi, la gravidanza gemellare è poco frequente nell’uomo, infatti, meno del 2% delle gravidanze umane…