Aumenta la domanda a discapito dell’offerta. Secondo i nuovi studi dell’University College di Londra, la richiesta globale di acido solforico aumenterà vertiginosamente da 246 a 400 milioni di tonnellate entro il 2040. Per il settore della mobilità sostenibile, agricolo e soprattutto alimentare, sarà un duro colpo.
| Indice dei contenuti |
La centralità dell’acido solforico nella società moderna
Lo zolfo, in particolare sotto forma di acido solforico H2SO4, per la società odierna è il cuore pulsante delle batterie al litio e dei fertilizzanti al fosforo naturali. Quest’ultimi, si ottengono dalla trattazione delle rocce fosfatiche o farina d’ossa con l’acido solforico. I concimi ottenuti sono essenziali per il processamento di terreni calcarei e per la concimazione di ortaggi, diverse tipologie di alberi da frutto e cereali.
Con l’arrivo della tecnologia verde e l’intensificazione dell’agricoltura, è stato spinto al limite l’utilizzo di questa preziosa risorsa. Ai prezzi già vertiginosi causati dal caro energia, a gravare ulteriormente sui portafogli delle famiglie è proprio la questione dell’acido solforico.
I problemi di produzione
Più dell’80% dello zolfo ha origine nel petrolio e nei gas naturali. Vengono raffinati e liberati dall’1% fino al 3% di zolfo, in base alla resa della raffinazione. Come si può immaginare, a seguito delle svariate problematiche climatiche e ambientali, è iniziato un processo di decarbonizzazione e transizione energetica, che porterà entro il 2050 ad un inesorabile diminuzione dell’utilizzo dei combustibili fossili e di conseguenza anche a una diminuzione della produzione di zolfo.
Altro punto a sfavore è la guerra russo-ucraina che ha incentivato l’Unione Europea ad abbandonare i gas naturali, a favore di energie pulite.
Metodo Frasch e torrefazione
Oltre il petrolio e i gas naturali, buona parte di zolfo viene ricavata dall’attività vulcanica o dall’estrazione dai giacimenti con il metodo Frasch, decisamente meno gettonato, dato il rincaro energetico e le complicazioni ambientali. Per la sua esecuzione, infatti, sono necessarie tonnellate d’acqua dalla temperatura di 160 gradi centigradi, in modo da fondere lo zolfo (con una temperatura di fusione di 120 gradi centigradi) e aria compressa, per riportare l’emulsione di acqua e zolfo in superficie. L’estrazione dei minerali di solfuro, inoltre, risulta estremamente pericolosa a causa della presenza di materiali pesanti come mercurio, tallio ed arsenico.
Per quanto riguarda la torrefazione, invece, abbiamo la produzione di anidride solforosa da trasformare istantaneamente in acido solforico, un processo rischioso e costoso.
Le conseguenze economiche
Aumenta la domanda, ancor di più i prezzi, ma diminuisce la produzione.
Con l’aumento del valore dell’acido solforico, abbiamo l’inevitabile innalzamento del prezzo dei beni alimentari che prevedono l’utilizzo di questa specie chimica per la loro concimazione. I più colpiti saranno i paesi in via di sviluppo. Analizzando la domanda e le previsioni per i prossimi decenni, sono stati forniti diversi scenari.
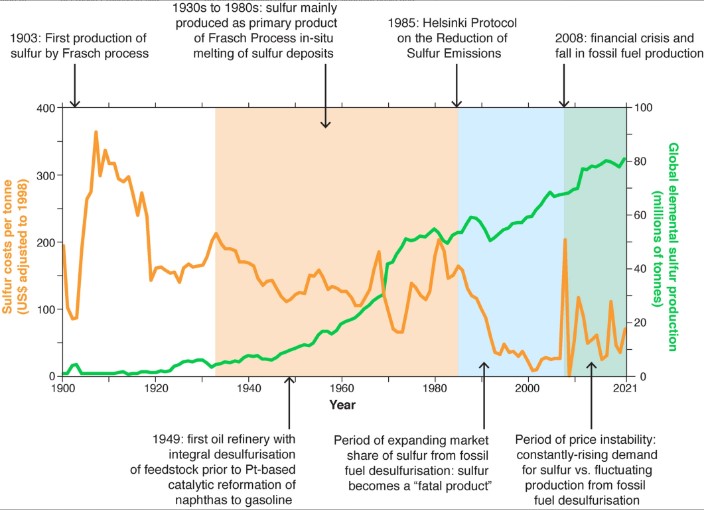
I grafici rimandano ad un deficit tra il 40% il 130% entro 2040. Circa 40 anni fa il prezzo dello zolfo si poteva considerare stabile ai 40$ per tonnellata, oggi date le diverse problematiche di natura ambientale e politica si prospetta un aumento oltre i 200$ per tonnellata.
Le alternative
L’aumento del prezzo dei beni alimentari (e non solo), può essere contrastato in più modi. Come precedentemente accennato, i vulcani sono una delle maggiori fonti di zolfo. La United States Geological Survey (USGS) ha rilevato in essi una fornitura praticamente illimitata di giacimenti di zolfo elementare e minerali di solfuro. L’unica nota dolente sono le emissioni provocate dal processo di estrazione.
Il piano B prevede l’utilizzo di alcuni batteri membri attivi del ciclo dello zolfo, come lo Spirillum Volutans e specie appartenenti alla famiglia Thiorhodaceae. Quest’ultimi attraverso un pigmento nominato bacteriopurina, possono scindere l’acido solfidrico con conseguente formazione di zolfo elementare.
2H2S + CO2 → (CH2O) + H2O + S2
Entrambe le modalità richiedono tempo, ricerca e in particolare, nell’ultimo caso, una sperimentazione su scala industriale.
Da quanto fin qui espresso, non resta che affidare alla scienza il futuro di questo prezioso materiale.
Asia Arezzio
Bibliografia:
https://rgs-ibg.onlinelibrary.wiley.com/doi/10.1111/geoj.12475
https://rgs-ibg.onlinelibrary.wiley.com/doi/10.1111/geoj.12475
