Innumerevoli titoli sensazionalistici si sono susseguiti, su giornali e riviste non strettamente scientifiche, durante questa emergenza: dalle possibili panacee per tutti i mali alle cure più bizzarre, spesso risulta difficile orientarsi con cognizione di causa in questo labirinto di informazioni.
Oggi parliamo di tutte le novità in campo terapeutico e cerchiamo di comprendere quali potrebbero essere i farmaci più promettenti.
Sarilumab e siltuximab
Come ormai abbiamo imparato, la COVID-19 ha qualcosa in comune con l’artrite reumatoide (AR), patologia infiammatoria che colpisce le articolazioni. Già la scienza ha preso in prestito da questa malattia un farmaco, il tocilizumab, che già ha mostrato qualche risultato interessante, alcuni ancora non pubblicati, sopratutto nei pazienti gravi.
Se per il sarilumab ancora siamo agli albori, cosa ha spinto l’Aifa (Agenzia Italiana del Farmaco) ad approvare studi a riguardo?
Entrambi (come potete notare anche dalla somiglianza dei nomi) sono anticorpi monoclonali: altro non sono che proteine prodotte in laboratorio, le quali legano specifiche molecole responsabili delle patologie delle quali stiamo parlando, in questo caso il recettore dell’interleuchina 6 (IL-6). Quest’ultima è una citochina (proteina prodotta in corso di infiammazione) che è molto rappresentata in pazienti affetti sia da AR che da COVID-19: per agire, l’IL-6 deve legare a sua volta il suo recettore, in modo tale da innescare processi che portano al proseguire dell’infiammazione e del danno a tessuti.
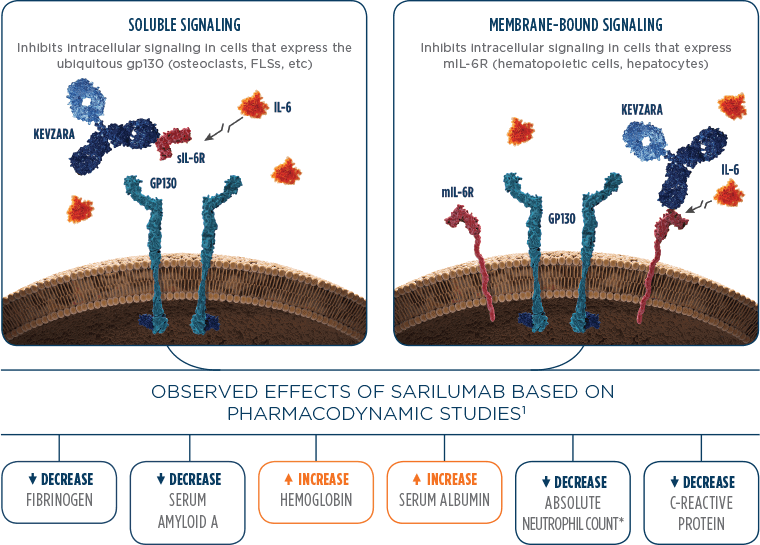
Questo aumento ingente delle citochine si verificherebbe soprattutto nei pazienti più gravi, che ad oggi devono pertanto affidarsi a farmaci in sperimentazione.
Attualmente sono in corso due studi: uno pilota su un piccolo numero di pazienti e senza confronto con altre terapie, e uno molto più ampio (AMMURAVID) nel quale saranno confrontati ben 7 diversi protocolli terapeutici. Tra questi spunta anche il siltuximab, che agisce direttamente contro l’IL-6.
L’ormai assodata intuizione sulla correlazione alto grado di infiammazione-gravità della COVID19 fa ben sperare: oltre – chiaramente – al meccanismo comune con l’ormai noto Tocilizumab.
Baricitinib
Altro farmaco in prestito dall’artrite reumatoide. Senza scendere troppo nei dettagli, questa volta il meccanismo è un po’ diverso: innanzitutto il farmaco è somministrabile anche per bocca (i precedenti sono utilizzati endovena); inoltre, agisce dopo che il legame molecola-recettore è già avvenuto, bloccando questa volta piccole proteine (JAK), sempre coinvolte nella sintesi delle citochine infiammatorie.
Il vantaggio potrebbe risiedere nella maggiore maneggevolezza; inoltre, se i precedenti si focalizzano solo su IL-6 e il suo recettore, le proteine JAK si trovano coinvolte in molti altri meccanismi che causano infiammazione, nonché (come abbiamo imparato) il peggioramento del paziente. Una sorta di effetto multiplo che potrebbe risultare più efficace.
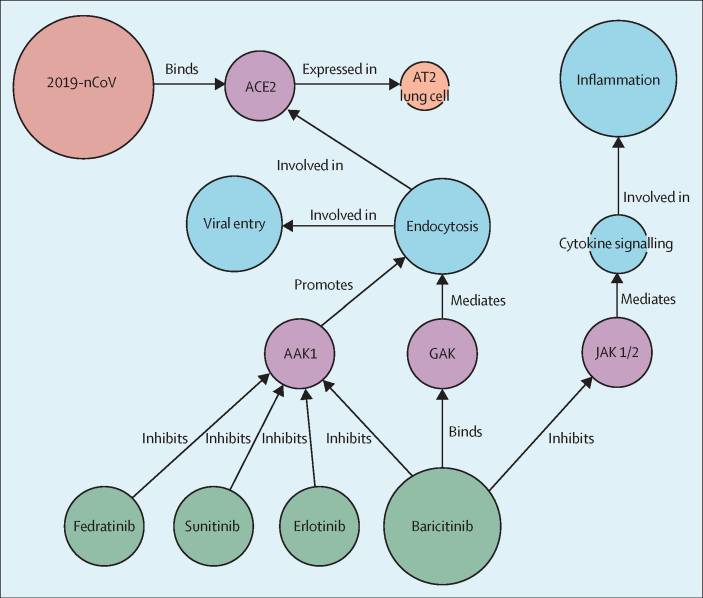
Ma c’è di più. Secondo uno studio pubblicato su Lancet, questo farmaco agirebbe anche su un altro fronte: l’ingresso del virus nella cellula. Come è ormai noto, la porta di ingresso del virus è il recettore ACE2: l’entrata del virus è tuttavia possibile solo se interviene anche un’altra proteina (AAK1) la cui funzione è inibita dal baricitinib.
Insomma, un’intuizione non da poco che, se si dimostrerà efficace, agirà su più fronti rispetto ad altri farmaci attualmente in possesso. Non a caso, l’Aifa ha autorizzato due studi, dei quali uno è il già citato AMMURAVID.
Selinexor
Questa volta cambiamo tipologia di farmaco: il selinexor è stato recentemente approvato negli USA nella terapia di casi molto resistenti di mieloma multiplo, tumore di interesse ematologico (ovvero che coinvolge cellule sanguigne, nello specifico le plasmacellule). L’approvazione è stata addirittura accelerata, in quanto questi pazienti non rispondono ad altre terapie e il farmaco si è dimostrato abbastanza efficace.
Ma cosa hanno in comune un’infezione virale ed un tumore?
Sembrerebbe strano tentare di utilizzare lo stesso farmaco, ma il selinexor induce la morte cellulare (apoptosi) delle cellule tumorali, così come potrebbe indurla nelle cellule infettate dal virus. Qualche cenno al meccanismo: anche qui abbiamo una doppia azione, mediata dall’inibizione di un processo chiamato “esportazione nucleare“; questa è svolta, tra le altre proteine, dall’esportina 1.
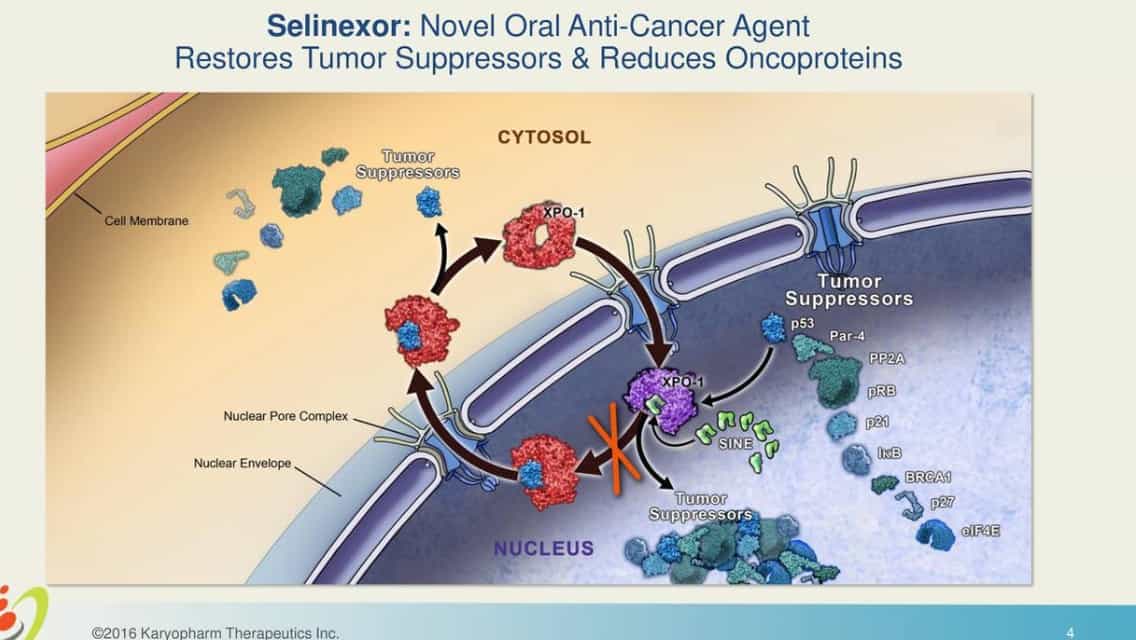
Quanto le proteine implicate nell’infiammazione, tanto quelle virali hanno bisogno dell’esportina 1 per svolgere la loro funzione correttamente. Da questo dato, è stato impostato uno studio che coinvolge 40 centri a livello internazionale.
Piccola nota sull’AMMURAVID: tutti i farmaci testati saranno associati alla terapia standard (idrossiclorochina) e confrontati non solo tra loro, ma anche con l’uso della sola idrossiclorochina stessa. Per questo motivo, lo studio promosso dalla Società Italiana di Malattie Infettive e Tropicali, potrebbe fornire informazioni molto interessanti per focalizzare la ricerca sulle cure realmente migliori rispetto ad altre, selezionando il farmaco più efficace.
Nell’attesa che questi studi dimostrino – come ci auguriamo – l’efficacia di nuove terapie, una cosa è certa: la scienza non si ferma, nemmeno di fronte ad un virus e ad una malattia totalmente nuovi.
Quello che possiamo fare attualmente, essendo il vaccino un’opzione più tardiva, è affinare al meglio la strategia terapeutica, grazie a due elementi fondamentali: l’intuito e le conferme inequivocabili dei dati scientifici.
Emanuele Chiara
Bibliografia:
https://www.aifa.gov.it/sperimentazioni-cliniche-covid-19
https://onlinelibrary.wiley.com/doi/abs/10.1002/jmv.25964
https://www.ncbi.nlm.nih.gov/pmc/articles/PMC7137985/
